乙酰苯胺的制备化学实验
乙酰苯胺,学名N-苯(基)乙酰胺,白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体。

1.掌握由苯胺乙酰化制备乙酰苯胺的原理和方法。
2.掌握分馏的原理及分馏装置的安装和操作。
3.巩固重结晶的操作方法。
实验原理反应式:
芳胺的酰化在有机合成中的作用:
(1)乙酰化反应常被用来“保护”伯胺和仲胺官能团,以降低芳胺对氧化性试剂的敏感性。
(2)氨基经酰化后,降低了氨基在亲电取代反应(特别是卤化)中的活化能力,使其由很强的第I类定位基变成中等强度的第I类定位,使反应由多元取代变为有用的一元取代。
(3)由于乙酰基的空间效应,往往选择性地生成对位取代产物。
(4)在某些情况下,酰化可以避免氨基与其它功能基或试剂(如RCOCl,-SO2Cl,HNO2等)之间发生不必要的反应。
作为氨基保护基的酰基基团可在酸或碱的催化下脱除。
芳胺可用酰氯、酸酐或冰醋酸加热来进行酰化,使用冰醋酸试剂易得,价格便宜,但需要较长的反应时间,适合于规模较大的制备。虽然乙酸酐一般来说是比酰氯更好的酰化试剂,但是当用游离胺与纯乙酸酐进行酰化时,常伴有二乙酰胺[ArN(COCH3)2]副产物的生成。
反应方程式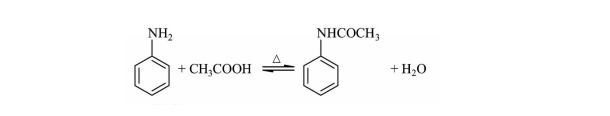
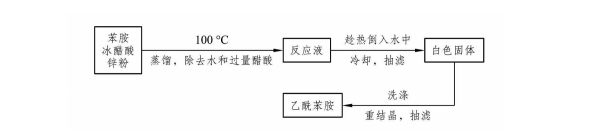
1.投料:
在25mL圆底烧瓶中,加入10mL苯胺、1.5mL冰醋酸及少许锌粉(约0.01g)然后装上一短的刺形分馏柱,其上端装一温度计,支管通过支管接引管与接受瓶相连,接受瓶外部用冷水浴冷却。
2.反应
将圆底烧瓶在石棉网上用小火加热,使反应物保持微沸约15min。然后逐渐升高温度,当温度计读数达到100℃左右时,支管即有液体流出。维持温度在100~110℃之间反应约1.5h,生成的水及大部分醋酸已被蒸出
3、分离提纯,此时温度计读数下降,表示反应已经完成。在搅拌下趁热将反应物倒入10mL水中,冷却后抽滤析出的固体,用冷水洗涤。粗产物用水重结晶,产量0.6~0.9g,熔点113~114℃(文献值114.3℃)。
注意事项(1)久置的苯胺易被氧化,故最好用新蒸的苯胺。
(2)加人锌粉的目的是防止苯胺在反应过程中被氧化,生成有色杂质。
(3)反应液冷却后,立即析出固体产物,粘在瓶壁上,不易处理。故应趁热在搅动下倒人冷水中,以除去过量的醋酸及未反应的苯胺。
急救措施皮肤接触:脱去污染的衣着,用流动清水冲洗。
眼睛接触:立即翻开上下眼眼睑,用流动清水冲洗15分钟。就医。
吸入:脱离现场至空气新鲜处。就医。
食入:误服者给饮足量水,催吐。就医。
灭火方法选自.网上补课 www.dushuv.com :雾状水、泡沫、二氧化碳、干粉、砂土。
智能推荐
- 下一篇:化学元素周期表读音和口诀 押韵
- 上一篇:摩尔质量怎么算